Het eerste patiëntonderzoek met een mogelijk MD-medicijn in Nederland is in volle gang. Arts-onderzoeker Joost Kools test het middel DYNE-101 in het Radboudumc op zeven patiënten. Hij vertelt hoe dat gaat en licht de tussentijdse resultaten toe. ‘Het middel kan op zijn vroegst in 2030 voor alle MD’ers beschikbaar worden, áls het beschikbaar wordt.’
De eerste resultaten met het middel DYNE-101 zijn hoopgevend, berichtte fabrikant Dyne dit voorjaar. Wat krijgt dit middel voor elkaar? ‘Ik mag niet meer vertellen dan wat Dyne zelf deelt. In een presentatie in mei liet het bedrijf zien dat het middel verbeteringen geeft in bijvoorbeeld spierkracht, loopsnelheid, vermoeidheid, darmklachten en dagelijkse activiteit. Op moleculair niveau doet het wat het moet doen en de myotonie neemt al bij lage dosering merkbaar af: deelnemers kunnen hun gespannen vuist enkele seconden sneller weer ontspannen. De bijwerkingen vallen mee en gaan vaak vanzelf over. Voor sommige bijwerkingen, zoals een allergische reactie, kunnen we aanvullende medicatie geven.’
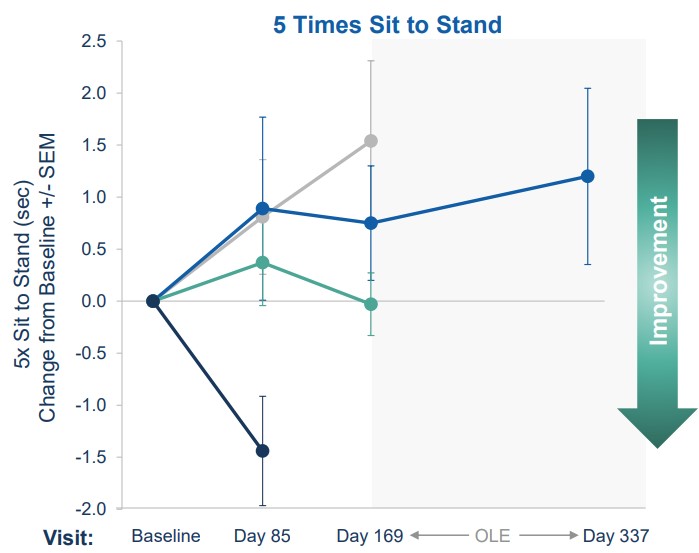
Deelnemers kunnen bijvoorbeeld 0,6 seconden sneller 10 meter lopen, of doen er zo’n 1,5 seconden korter over om vijf keer op te staan vanuit zitten. Wat betekent dat? ‘Je wilt dat medicijnen een gunstig effect hebben op het dagelijks leven van de patiënt. Je zou bijvoorbeeld willen dat iemand die nu niet kan opstaan na een val, dat wel kan met dit medicijn. Maar dat weten we nog niet. We meten voor en tijdens het onderzoek allerlei dingen die samenhangen met MD en die we heel goed kunnen meten. Zo trekken of duwen deelnemers in een speciaal instrument zo hard mogelijk aan een meetapparaat. We kunnen in dat apparaat precies meten hoeveel kracht ze daarbij uitoefenen. Dat is een maat voor spierkracht. In de vragenlijst MD Health Index vullen deelnemers in hoe ze onder meer hun vermoeidheid, darmklachten en activiteit ervaren.’
Het farmaceutische bedrijf Dyne deelt hoopvolle resultaten terwijl het onderzoek nog loopt. Is dat bijzonder? ‘We zien tegenwoordig vaker dat een medicijnenfabrikant tussentijdse resultaten deelt, zeker beursgenoteerde bedrijven zoals Dyne doen dat. Positief nieuws biedt de kans dat het middel sneller beschikbaar komt. Dyne kan met de autoriteiten in gesprek gaan die beslissen over toelating van medicijnen tot de markt. In Amerika is dat de FDA, in Europa de EMA. Als Dyne met hen mag bespreken welke stappen nodig zijn om het medicijn te kunnen toelaten, kan Dyne die zo snel mogelijk realiseren. Er zijn sinds kort regels waardoor nieuwe medicijnen voor ziekten waarvoor nog geen behandeling is in een snel-traject terecht komen als ze goede tussenresultaten laten zien. Deze medicijnen kunnen dan sneller beschikbaar worden voor patiënten.’
Wanneer komt het middel beschikbaar als het inderdaad goed werkt? ‘Ik denk dat dat op zijn vroegst in 2030 kan, áls het middel inderdaad goed blijkt te werken in al het onderzoek. Het onderzoek dat we nu doen is een fase I/II-studie, die de werkzaamheid per dosis moet laten zien. De tussentijdse resultaten laten een duidelijk verschil zien tussen de laagste en de wat verhoogde dosering. In de zomer van 2027 is dit onderzoek afgerond: dan weten we bij welke dosis het medicijn het beste werkt, zonder dat het te veel bijwerkingen geeft.
‘Daarna moet er nog een vervolgonderzoek plaatsvinden om die optimale dosis te testen bij een grotere groep patiënten. Traditioneel gebeurde dat in een grote, internationale fase III-studie, tegenwoordig zien we ook dat bedrijven de huidige fase I/II studies uitbreiden tot een soort fase III-studie. Meestal duurt dat ongeveer een jaar. Als dat goed gaat en FDA en EMA zouden het middel zo snel mogelijk tot de markt toelaten, moet Nederland nog besluiten of zorgverzekeraars het gaan vergoeden. Dat duurt vaak ook zo’n twee jaar.’
Waarom duurt het onderzoek zo lang? ‘In juli 2023 kreeg de eerste patiënt het middel of een placebo, in de maanden daarna volgden stap voor stap de andere zes deelnemers bij Radboudumc. Wereldwijd doen zo’n 60 mensen mee, verdeeld over vier groepen die een verschillende dosis van het middel krijgen. Als een medicijn voor het eerst in mensen wordt getest, gaat het verhogen van de dosering vaak stapsgewijs. Eerst willen we zien dat het medicijn veilig is in de laagste dosering, voordat de volgende dosering wordt getest in het volgende groepje patiënten.’
Wat gebeurt er precies in het onderzoek dat nu loopt? ‘Eerst krijgen de deelnemers 24 weken lang het middel of een placebo – een nepmedicijn. Arts en patiënten weten niet wie het middel en wie het placebo-middel krijgen. Na die 24 weken krijgen alle deelnemers 24 weken het medicijn toegediend via een infuus. Dat kan elke vier of acht weken zijn, afhankelijk van de groep waar ze zijn ingedeeld. Daarna begint de lange-termijn-extensiefase: de deelnemers krijgen nog bijna twee jaar lang het middel toegediend, maar er vinden veel minder metingen plaats. Soms wordt de dosering in deze periode aangepast naar de optimale dosering. In de zomer van 2027 sluit de laatste deelnemer deze periode af. Als alle resultaten daarna zijn geanalyseerd, is het onderzoek afgerond. Tenzij Dyne de studie verlengt met extra groepen.’
Komt er ook gauw onderzoek onder kinderen, zodat zij het middel zo snel mogelijk kunnen krijgen? ‘Natuurlijk wil iedereen, ook de fabrikant, het medicijn zo snel mogelijk voor kinderen beschikbaar maken. Kinderen met MD zijn vaak zieker, voor hen valt er nog meer te winnen. Maar hoe doe je dat veilig? Over het algemeen worden medicijn eerst op volwassenen getest, voordat de kinderen aan de beurt zijn. Dit doen we omdat we dan een beter beeld hebben van de risico’s en mogelijke voordelen van een medicijn. Hierdoor hoeven we de kinderen niet onnodig te belasten of bloot te stellen aan risico’s. Daarnaast zijn onderzoeken in volwassenen vaak makkelijker en betrouwbaarder uit te voeren, waardoor de kans op succes groter is.’
Is dit het eerste middel tegen MD dat onderzocht wordt? ‘Nee, fabrikant Avidity heeft fase I/II al afgerond voor een ander medicijn: Del-disiran (OAC 1001) dat op ongeveer dezelfde manier werkt als Dyne-101 en tot nu toe vergelijkbare resultaten laat zien. Er is in overleg met de Amerikaanse FDA al goedkeuring voor een versneld traject naar toelating tot de markt. Rond november gaan we in Radboudumc en in Maastricht UMC+ elk zo’n tien patiënten werven voor dit onderzoek.
Kan het middel Del-disiran veel sneller beschikbaar komen voor Nederlandse MD-patiënten dan Dyne-101? ‘Ik verwacht dat het onderzoek eind 2026 helemaal is afgerond. Dan zijn rond half 2027 resultaten bekend en kunnen FDA en EMA het medicijn toelaten tot de markt. Daarna doet Nederland er naar verwachting nog zo’n twee jaar over om te bepalen of het middel wordt opgenomen in de zorgverzekering. Dan is het 2029.’
> In november 2024 worden MD-patiënten uitgenodigd voor onderzoek naar een ander medicijn. Lees mijn artikel daarover: Binnenkort: nieuw patiëntonderzoek in Nederland naar vergevorderd MD-medicijn.
> Lees het interview met Onno, deelnemer aan het onderzoek naar Dyne-101. ‘Op het fysieke deel van de trial had ik me best aardig voorbereid. Wat ik heb onderschat, is dat het ook psychisch zwaar kan zijn.’ Spierfonds, september 2024.
> Meer weten over MD? Op de website van stichting MD Nederland staat veel informatie.
Ik schreef dit artikel uit persoonlijke interesse, omdat MD bij mij in de familie voorkomt.

